ประกาศวันหยุด
ประจำเดือน มิถุนายน 2569
วันจันทร์ที่ 1 มิถุนายน 2569
(วันหยุดชดเชยวันวิสาขบูชา)
วันพุธที่ 3 มิถุนายน 2569
(วันเฉลิมพระชนพรรษา สมเด็จพระนางเจ้าสุทิดา พัชรสุธาพิมลลักษณ พระบรมราชินี)

Central
Research
Ethics
Committee
คณะกรรมการกลางพิจารณาจริยธรรมการวิจัยในคน (CREC Thailand)

เรียน นักวิจัย เเละผู้ประสานงานวิจัย
ขอความอนุเคราะห์ผู้วิจัย/ผู้ประสานงานวิจัย
ส่งรายชื่อผู้ประสานงานของโครงการที่ท่านกำกับดูแล
(รายชื่อผู้ประสานงานในระบบ Submission Online)
** เพื่อการขอรายชื่อผู้ประสานงานโครงการวิจัยมีวัตถุประสงค์เพื่อกำหนดผู้รับผิดชอบในการติดต่อและประสานงานของโครงการให้ชัดเจน สนับสนุนการดำเนินงานวิจัยให้เป็นไปอย่างมีประสิทธิภาพ ต่อเนื่อง และสอดคล้องตามแผนการศึกษา รวมทั้งเพื่อให้สามารถติดตาม ตรวจสอบ และอ้างอิงข้อมูลการดำเนินงานได้อย่างถูกต้อง และตรวจสอบย้อนกลับได้
**รบกวนตั้งชื่อไฟล์เอกสารเป็นรหัสโครงการที่รับผิดชอบ เเละนำส่งเอกสารไปที่อีเมล official@crecthailand.org

ประกาศวันหยุด
ประจำเดือน มิถุนายน 2569
วันจันทร์ที่ 1 มิถุนายน 2569
(วันหยุดชดเชยวันวิสาขบูชา)
วันพุธที่ 3 มิถุนายน 2569
(วันเฉลิมพระชนพรรษา สมเด็จพระนางเจ้าสุทิดา พัชรสุธาพิมลลักษณ พระบรมราชินี)

Central
Research
Ethics
Committee
คณะกรรมการกลางพิจารณาจริยธรรมการวิจัยในคน (CREC Thailand)

เรียน นักวิจัย เเละผู้ประสานงานวิจัย
ขอความอนุเคราะห์ผู้วิจัย/ผู้ประสานงานวิจัย
ส่งรายชื่อผู้ประสานงานของโครงการที่ท่านกำกับดูแล
(รายชื่อผู้ประสานงานในระบบ Submission Online)
** เพื่อการขอรายชื่อผู้ประสานงานโครงการวิจัยมีวัตถุประสงค์เพื่อกำหนดผู้รับผิดชอบในการติดต่อและประสานงานของโครงการให้ชัดเจน สนับสนุนการดำเนินงานวิจัยให้เป็นไปอย่างมีประสิทธิภาพ ต่อเนื่อง และสอดคล้องตามแผนการศึกษา รวมทั้งเพื่อให้สามารถติดตาม ตรวจสอบ และอ้างอิงข้อมูลการดำเนินงานได้อย่างถูกต้อง และตรวจสอบย้อนกลับได้
**รบกวนตั้งชื่อไฟล์เอกสารเป็นรหัสโครงการที่รับผิดชอบ เเละนำส่งเอกสารไปที่อีเมล official@crecthailand.org

ประกาศวันหยุด
ประจำเดือน มิถุนายน 2569
วันจันทร์ที่ 1 มิถุนายน 2569
(วันหยุดชดเชยวันวิสาขบูชา)
วันพุธที่ 3 มิถุนายน 2569
(วันเฉลิมพระชนพรรษา สมเด็จพระนางเจ้าสุทิดา พัชรสุธาพิมลลักษณ พระบรมราชินี)


คณะกรรมการกลางพิจารณาจริยธรรมการวิจัยในคน (CREC Thailand)
เป็นหน่วยงานกลางรับพิจารณาโครงการวิจัยแบบพหุสถาบัน โดยมีคณะกรรมการกลางที่จัดตั้งขึ้นเพื่อพิจารณาการขอจริยธรรมการวิจัยในคน อยู่ภายใต้การกำกับดูแลของมูลนิธิส่งเสริมการวิจัยในคนของประเทศไทย (มสจท)
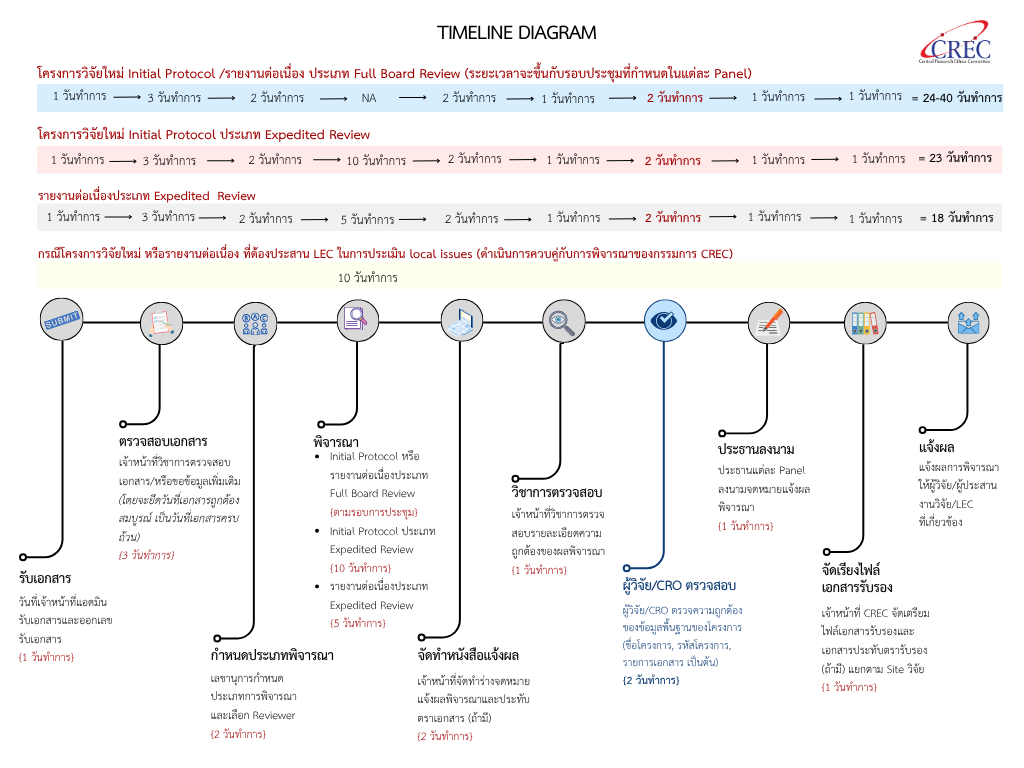
Milestones



คณะกรรมการกลาง
หลักการทำงานที่เราเชื่อมั่น

รับผิดชอบ
การวิจัยพหุสถาบัน ดำเนินหน้าที่ด้วยความรับผิดชอบต่อสังคม โดยยึดหลักจริยธรรม ความโปร่งใสและผลประโยชน์ของผู้เข้าร่วมวิจัยเป็นสำคัญ

โปร่งใส
คณะกรรมการกลางยึดหลักความโปร่งใสในการพิจารณาและตัดสินใจ เพื่อสร้างความไว้วางใจจากทุกภาคส่วน ตรวจสอบได้ทุกขั้นตอน

มีประสิทธิภาพ
ดำเนินงานอย่างมีประสิทธิภาพด้วยกระบวนการที่เป็นระบบรวดเร็วเพื่อให้การพิจารณาจริยธรรมการวิจัยในคนเป็นไปอย่างรอบคอบและได้มาตรฐาน

ปกป้องสิทธิ
เพื่อให้การพิจารณาการขอจริยธรรมการวิจัยเป็นไปอย่างรอบคอบปลอดภัยและความเป็นอยู่ที่ดีของผู้เข้าร่วมการวิจัย

ภาคี MOU




คณะกรรมการกลางพิจารณาจริยธรรมการวิจัยในคน
สนับสนุนการพัฒนางานวิจัยในประเทศไทยให้เป็นไปตามหลักจริยธรรม มาร่วมเป็นส่วนหนึ่งในการยกระดับคุณภาพการวิจัยพหุสถาบันงานไทยให้ก้าวไกล ด้วยกระบวนการพิจารณาที่โปร่งใสมีจริยธรรม และเป็นที่ยอมรับในระดับสากล
Working Time:
จันทร์-ศุกร์ เวลา 08.30-16.30 น.
Tel.:
Email :

เสนอเเนะ/ติชม

คำถามที่พบบ่อย
1.Sponsor/Lead PI สามารถส่ง 6M LL and DMC letter ให้ทาง CREC พิจารณาได้
2.สำหรับเอกสาร safety (Local SAE, individual CIOM) ที่ทาง local EC ประเมินแล้ว และ มีการแจ้งให้ take action เช่น ถูกตัดสิน site visit/suspension/termination of approval อันเป็นผลมาจากเหตุการณืนี้ >> อันนี้จะขอให้รายงาน CREC ร่วมด้วย ภายในระยะเวลาที่กำหนด
3.ในกรณี Individual CIOMS ที่ ทาง sponsor เและ PI เห็นเห็นตรงกันว่าจะต้อง take action ในทันที เนื่องจากมีความเสี่ยงต่อ ความปลอดภัยของอาสาสมัครขั้นรุนแรง จะสามารถดำเนินการได้ทันที พร้อมกับดำเนินการ report CREC เพื่อรับทราบ
4.SOP ฉบับ 5.0 วันที่ 31 ตุลาคม 2566 ได้ระบุว่า รายงานเหตุการณ์ไม่พึงประสงค์ชนิดร้ายแรงที่เกิดขึ้นกับอาสาสมัครในสถาบันที่ทำวิจัย (local SAE/SUSAR) ที่ผู้สนับสนุนการวิจัยประเมินแล้วว่าน่าจะสัมพันธ์ (Probably related) หรือสัมพันธ์ (definitely related) กับยาวิจัยและเพิ่มความเสี่ยงต่ออาสาสมัครโดยเร็ว ภายใน 15 วันปฏิทิน หลังทราบผลการประเมินความสัมพันธ์กับยาวิจัย แต่รายงานเหตุการณ์ไม่พึงประสงค์ชนิดร้ายแรงที่ไม่คาดคิดที่เกิดในสถาบัน (local SUSAR) ที่บริษัท เป่ยจีน ได้จัดทำขึ้นมีประเมินความสัมพันธ์ระหว่างรายงานเหตุการณ์ไม่พึงประสงค์กับยาวิจัย โดยสรุปว่าเหตุการณ์ดังกล่าวมีความสัมพันธ์ (related) กับยาวิจัย แต่ไม่ระบุประเภทของความสัมพันธ์ โดยทาง CREC เห็นว่าการส่งขอพิจารณา เอกสาร Local Safety report มาให้คณะกรรมการพิจารณา เป็นรายงานที่ไม่เข้าข่ายการพิจารณาของ CREC จึงไม่ต้องส่งเอกสาร local SUSAR ที่ Sponsor สรุปว่าเหตุการณ์ดังกล่าวมีความสัมพันธ์ (related) กับยาวิจัย ให้ทาง CREC ตามหลักเกณฑ์ที่ CREC SOP กำหนดไว้
โครงการวิจัยจะเข้าข่ายการพิจารณาด้านจริยธรรมการวิจัยและกำกับดูแลโดย คณะกรรมการกลางฯ หากมีคุณสมบัติตรงตาม**เช็คลิสต์ข้อใดข้อหนึ่ง**ดังต่อไปนี้ค่ะ
1. เป็นการทดลองทางคลินิกพหุสถาบันของผู้ผลิตเภสัชภัณฑ์** (Pharmaceutical-sponsored multi-center clinical trial)
2. เป็นโครงการศึกษาวิจัยพหุสถาบัน (Multicenter study)** ของนักวิจัยที่วางแผน ยื่นขอ หรือได้รับทุนสนับสนุนจาก**หน่วยงานภาครัฐหรือองค์กรสาธารณะ** เช่น สำนักงานการวิจัยแห่งชาติ (วช.), สำนักงานกองทุนสนับสนุนการสร้างเสริมสุขภาพ (สสส.), สถาบันวิจัยระบบสาธารณสุข (สวรส.), สมาคมวิชาชีพ, ราชวิทยาลัย หรือมูลนิธิ เป็นต้น
3. เป็นโครงการศึกษาวิจัยศูนย์เดียว แต่มีการเก็บข้อมูลในหลายแห่ง** (Single center, multi-sites study) โดยเป็นโครงการของนักวิจัยในสถาบันภาคี และมีผู้วิจัยร่วมประจำอยู่ในแต่ละสถานที่เก็บข้อมูล (site) นั้นๆ
**หมายเหตุ:** หากโครงการวิจัยของคุณมีคุณสมบัติ**ตรงกับข้อใดข้อหนึ่ง**ในเช็คลิสต์ข้างต้น จะถือว่าอยู่ในขอบเขตการพิจารณารับรองด้านจริยธรรมของคณะกรรมการกลางฯ

https://drive.google.com/file/d/134RZWxU7BNM7aIiJI0BYdHpHt8VaNF0a/view
บทความ & ข่าวสาร
ขอบคุณสำหรับการเยี่ยมชมเว็บไซต์
0+
- หน้าแรก หน้าแรก
- เกี่ยวกับเรา เกี่ยวกับเรา
- ความร่วมมือ ความร่วมมือ
- ประกาศและคำสั่ง ประกาศและคำสั่ง
- การปฏิบัติงาน การปฏิบัติงาน
- การยื่นโครงการ การยื่นโครงการ
- ปฏิทิน ปฏิทิน
- ข่าวสารประชาสัมพันธ์ ข่าวสารประชาสัมพันธ์
- ติดต่อและคำถามที่พบบ่อย ติดต่อและคำถามที่พบบ่อย
- แบบฟอร์มรับเรื่องร้องเรียนและปัญหาการดำเนินงาน แบบฟอร์มรับเรื่องร้องเรียนและปัญหาการดำเนินงาน
- คู่มือการใช้งานระบบ Submission Online คู่มือการใช้งานระบบ Submission Online
- โครงการที่ผ่านการรับรองจาก CREC โครงการที่ผ่านการรับรองจาก CREC
- crec education crec education
ความร่วมมือ
ประกาศและคำสั่ง
การปฏิบัติงาน
การยื่นโครงการ
ปฏิทิน
ติดต่อและคำถามที่พบบ่อย







